每经数说丨1月上半月新药研发:国内将迎首款CAR-T产品、百济神州与诺华合作PD-1产品
◎1月上半月,百济神州与诺华达成合作开发替雷利珠单抗,总金额超22亿美元。还值得关注的是,复星凯特阿基仑赛注射液上市申请进入行政审批,或成国内首款CAR-T产品。
每经记者 金喆 每经编辑 魏官红

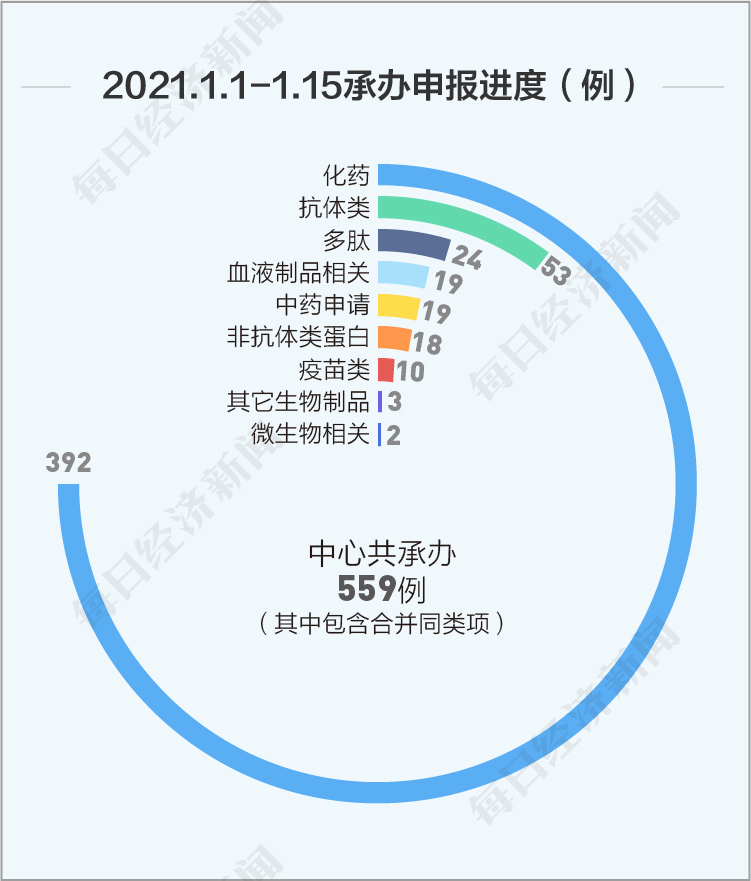
丁香园Insight数据库援引国家药品监督管理局药品审评中心数据显示,1月1日~1月15日,中心共承办559例申报进度,其中受理化药申请392项,抗体类53项,多肽24项,血液制品相关19项,中药申请19项,非抗体类蛋白18项,疫苗类10项,其它生物制品3项,微生物相关2项。
本阶段创新药有以下突破:
首先,百济神州与诺华达成合作开发替雷利珠单抗,总金额超22亿美元,创下目前中国国内单品种药物授权合作金额最高纪录。
第二,复星医药旗下复星凯特CAR-T产品阿基仑赛注射液的上市申请进入行政审批阶段,预计将在近期获批。如果获批,这将是国内首款CAR-T疗法产品。
第三,GSK艾滋病新药多替拉韦利匹韦林片国内报上市。
每月要闻
1、百济神州与诺华达成合作开发替雷利珠单抗,总金额超22亿美元
1月12日,百济神州宣布与诺华就其自主研发的PD-1抗体药物替雷利珠单抗在多个国家的开发、生产与商业化达成合作与授权协议,首付款高达6.5亿美元,总交易金额超过22亿美元。
百济神州中国区总经理兼公司总裁吴晓滨在1月12日下午公司召开的记者会上表示,公司如今在研产品众多,接下来会采用“两条腿走路”的方式:一方面要借助现有的资源与合作伙伴的力量;另一方面,“依然要走好一条道路,建立自己的核心竞争能力,也就是研发、生产和商业化的能力”。
根据协议,本次合作双方都将保留其自主开发产品联合替雷利珠单抗用药组合的全球商业化权利,并负责为各自用于评估替雷利珠单抗联合公司或第三方药物开展的临床试验提供资金。
对此,百济神州首席财务官兼首席战略官梁恒解释称,公司与诺华合作开发新的适应症将由谁来受益的问题,“要看我们产品替雷利珠单抗,是和哪个产品结合”。据他介绍,双方联合替雷利珠单抗的产品将由各自进行商业化并实现收益,替雷利珠单抗则按照协议在不同区域由双方分别获得收益。
每经稿件:诺华获得百济神州PD-1海外市场开发及商业化许可 双方仍可分别探索联合用药可能性
2、复星凯特阿基仑赛注射液上市申请进入行政审批,或成国内首款CAR-T产品
近日,复星医药旗下复星凯特CAR-T产品阿基仑赛注射液的上市申请进入行政审批阶段,预计将在近期获批。
阿基仑赛注射液属于3类治疗用生物制品,由复星凯特从吉利德子公司Kite制药引进的靶向CD19自体CAR-T细胞治疗产品Yescarta。Yescarta于2017年10月18日获得美国FDA批准上市,成为全球首款用于治疗复发/难治性大B细胞淋巴瘤的CAR-T细胞药品。
近年来,中国的CAR-T临床试验数量增长较快,目前已超过美国。《每日经济新闻》记者了解到,1月上半月有两款CAR-T创新药获批临床,申报企业分别为亘喜生物、恒润达生。Insight数据库显示,共有27家企业、40个与CAR-T疗法有关的申报进度。其中,药明巨诺的CD19靶向CAR-T细胞疗法JWCAR029进度仅次于阿基仑赛注射液,也有望在2021年获批上市。
但是,我国CAR-T研发同质化严重,研发集中在CD19和BCMA等热门靶点,适应症主要是淋巴瘤、白血病、骨髓瘤等血液肿瘤。
3、GSK艾滋病新药多替拉韦利匹韦林片国内报上市
近日,GSK/ViiV进口新药多替拉韦利匹韦林片上市申请获国家药品监督管理局受理,该药是一款HIV二联复方新药,由多替拉韦(dolutegravir)和利匹韦林(rilpivirine)以50mg/25mg规格组成。2017年11月,多替拉韦利匹韦林片获FDA批准上市,Insight数据库显示,2019年全球销售额4.68亿美元。
《每日经济新闻》记者了解到,目前抗HIV病毒的药物主要包括CCR5拮抗剂、融合抑制剂、逆转录酶抑制剂、整合酶抑制剂、蛋白酶抑制剂。为避免单一用药产生的抗药性,临床上大多采用以上三种或三种以上的药物联合使用。
Insight数据库显示,在2019年全球药品销售额TOP100中,HIV药物共占8席,其中以吉利德为首,拥有5个Top100 HIV药,分别为Biktarvy(比克恩丙诺)、Genvoya(艾考恩丙替)、Truvada(恩曲他滨/替诺福韦)、Odefsey和Descovy。强生和GSK各拥有1/2款,分别为Prezista/Prezcobix(达芦那韦/地瑞那韦)和Tivicay(多替拉韦)和Triumeq(多替阿巴拉米,多替拉韦/拉米夫定/阿巴卡韦)。总体来说,以二联和三联复方为主。
而在国内,HIV新药仍以进口为主。Insight数据库显示,目前含艾滋病适应症的化药新药中,38个项目为进口,10个项目为国产品种。国产品种中,仅前沿生物的艾博卫泰获批上市,真实生物的阿兹夫定和艾迪药业的ACC007已递交上市申请,其余均处于临床阶段。
每月数读
1、本期首次注册上市的品种有5个(同一品种不同规格计为1种),如下图所示,全部为化药仿制药。

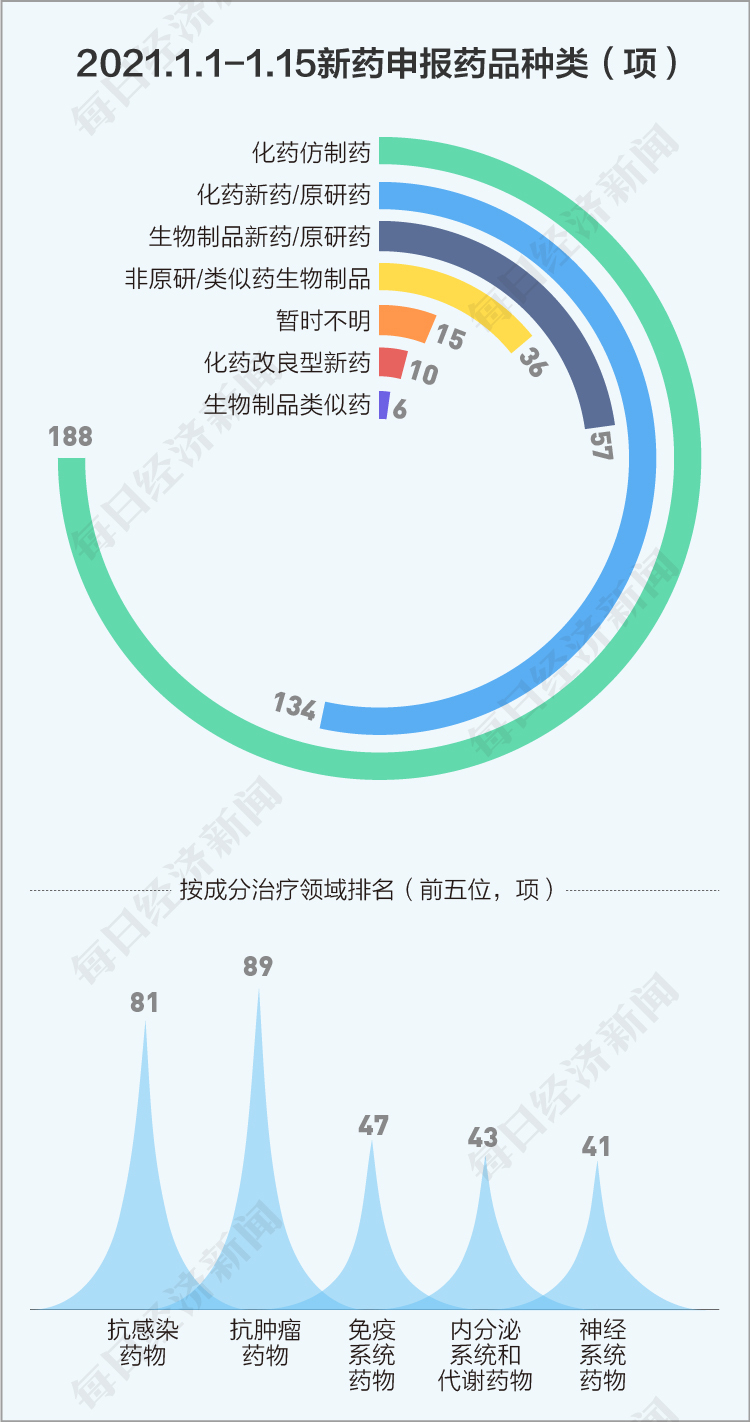
2、本阶段申报的项目中,化药仿制药188项,化药新药/原研药134项,生物制品新药/原研药57项,化药改良型新药10项,非原研/类似药生物制品36项,生物制品类似药6项,暂时不明15项。
按成分治疗领域排名,前五位是抗感染药物(81项),抗肿瘤药物(89项),免疫系统药物(47项),内分泌系统和代谢药物(43项)和神经系统药物(41项)。
本阶段无药物纳入优先审评审批品种。
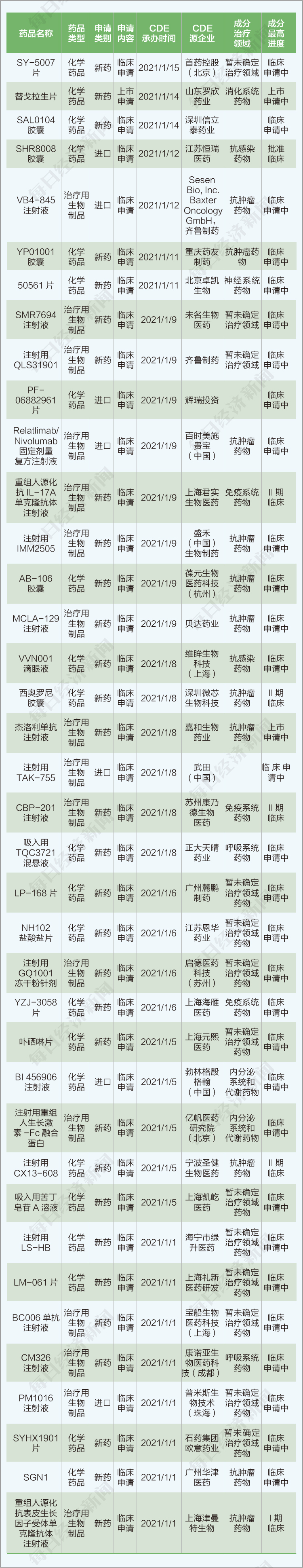
本阶段有30个创新药品种开展临床试验,其中,化学新药/原研药21个,生物制品新药/原研药9个。

3、本期共有一类注册新药临床申请37个(不含补充申请),上市申请1个,涵盖10家上市公司。
 每经头条
每经头条
 每经热评
每经热评















 川公网安备 51019002002025号
川公网安备 51019002002025号






